呼吸系统疾病与认知功能密切相关,慢阻肺病、睡眠呼吸疾病等均可引起认知功能障碍,而认知功能障碍也影响呼吸系统疾病诊治的依从性。2025年2月25日,中国医科大学附属第一医院王玮团队在Progress in Neuropsychopharmacology & Biological Psychiatry(IF = 5.3)发表综述,探讨了小胶质细胞衍生的小细胞外囊泡(sEV)在认知障碍中的关键作用。该综述基于细胞实验、动物研究及临床试验的证据,系统总结了M1和M2型小胶质细胞来源的sEV对认知障碍的影响,重点回顾了小胶质细胞来源sEV作为生物标志物的筛选与分离的研究进展,旨在为临床干预提供新的靶点和研究视角。

小胶质细胞在认知障碍中的影响
认知障碍可由神经系统疾病、神经退行性病变、全身性或精神疾病引发,影响患者的认知过程,包括思维、学习和记忆能力。患者通常表现出记忆丧失、意识混乱和判断力受损等症状,严重影响其日常生活和工作能力,对社会及家庭造成沉重经济负担。小胶质细胞是中枢神经系统(CNS)内的重要免疫细胞,在维持神经稳态及认知功能中发挥关键作用,在不同的发育阶段、生理区域和性别中表现出显著异质性。目前,小胶质细胞被分为四种亚型,分别是稳态小胶质细胞、疾病相关小胶质细胞(DAM)、过渡态小胶质细胞和双阴性小胶质细胞,其中DAM又被进一步分为促炎和抗炎亚型。M1型促炎小胶质细胞通过释放促炎因子介导免疫防御,而M2型抗炎小胶质细胞则分泌抗炎因子促进神经保护与修复。M1/M2平衡失调,尤其是M1型过度极化或M2型功能受损,可能加速认知障碍的发生与进展。近年来,细胞间通讯研究的进展使sEV成为关注热点。小胶质细胞来源sEV富含蛋白质、核酸及代谢物,可调控神经元信号通路,影响神经递质传递及氧化应激,并在神经炎症与细胞凋亡调控中发挥双重作用。随着对其在认知障碍中的作用机制研究不断深入,调控小胶质细胞sEV正被视为潜在的干预靶点。
小胶质细胞衍生的sEV在认知障碍中的作用机制
1、致病蛋白的跨膜运输
小胶质细胞来源的sEV可携带致病蛋白并促进其在脑内的聚集和传播,从而加剧神经毒性,如阿尔兹海默症中的Aβ和tau蛋白,或帕金森病中α-突触核蛋白。此外,sEV也可通过其膜上的TREM2依赖性结合Aβ,从而介导Aβ的清除,在AD早期缓解认知障碍。目前大多数研究集中在转运异常蛋白的致病机制,而对于有益作用研究较少。小胶质细胞外泌体缓解认知功能的机制研究对于减轻神经退行性疾病,尤其是疾病晚期,可能具有重要意义。
2、神经炎症
M1小胶质细胞来源的sEV包含促炎细胞因子如TNF-α、IL-6等,通过自分泌或旁分泌途径激活小胶质细胞,扩大神经炎症反应。病毒感染和重金属暴露也可诱导sEV释放来加剧神经炎症。M2型小胶质细胞释放的sEV可通过miRNA促进抗炎作用,改善神经炎症和认知功能。
3、血脑屏障(BBB)受损
炎症反应可导致BBB通透性增加,使纤维蛋白原等血源性成分进入脑内并激活小胶质细胞。小胶质细胞已被证明可以摄取并以sEV形式释放纤维蛋白原,形成正反馈环路,进一步损伤BBB结构并加剧神经炎症。另外,BBB中紧密连接蛋白的破坏与M1小胶质细胞sEV显著相关。相比之下,M2型小胶质细胞释放的sEV可上调紧密连接蛋白来增强BBB稳定性,在一定程度上缓解认知功能障碍。
4、神经元死亡
M1小胶质细胞sEV在神经元凋亡、铁死亡及自噬等细胞死亡过程中发挥关键作用,而抑制M1型小胶质细胞的激活并促进其向M2表型极化可有效保护神经元的数量及形态,凸显小胶质细胞sEV在神经调节中的重要作用。值得注意的是,与M1型小胶质细胞分泌的sEV共培养的神经元呈现典型铁死亡特征,而静息状态小胶质细胞分泌的sEV则不诱导神经元铁死亡,提示M1型小胶质细胞sEV可能为铁死亡相关认知障碍提供新的治疗靶点。
5、突触功能障碍
炎性条件下,小胶质细胞sEV抑制突触稳定性和树突棘形成,加剧兴奋性突触的丧失。在AD早期,富含Aβ的sEV与神经元的结合可以改变树突棘的形态和数量,削弱长时程增强作用(LTP),影响记忆形成。相较之下,M2型小胶质细胞EVs在保护突触和促进神经修复方面具有积极作用。sEV通过携带miRNA促进神经突生长和突触恢复,改善认知功能。
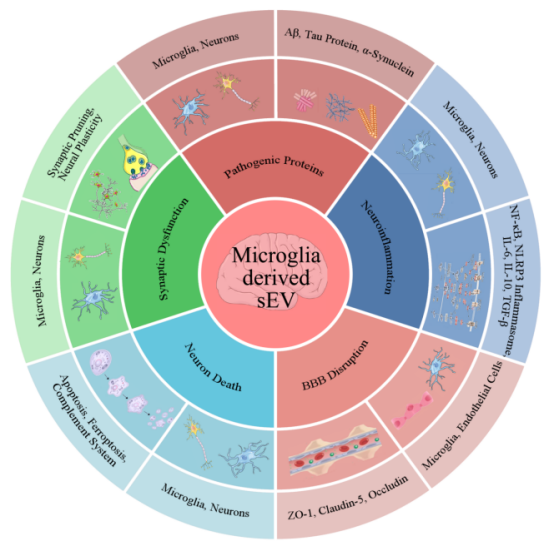
图1 小胶质细胞衍生的 sEV 在认知障碍中的作用
小胶质细胞来源的sEV在认知障碍诊断中的作用机制
小胶质细胞来源的sEV能够穿越BBB进入血液循环,使得脑源性sEV可在血浆中检测到。相较于脑脊液检测,血液检测具有更强的可操作性和非侵入性,为神经系统疾病的早期诊断提供了便利。由于神经退行性疾病发病隐匿,传统的PET/CT或认知行为测试(CBS)通常较晚进行,而sEV的血液检测可提供更早期的诊断线索。研究发现,血浆中小胶质细胞sEV携带的miR-132-5p、miR-125b-5p能精准区分AD患者与健康个体。其他miRNA如miR-29a-5p、miR-106b-5p可用于预测更广泛的认知障碍,包括轻度认知障碍(MCI)及AD早期阶段,从而延长干预窗口。值得注意的是,sEV的组成(蛋白质、核酸和miRNA等)会随疾病进展发生变化,因此可作为动态监测指标。此外,由于sEV在采样后仍能保持其生物学特性,其稳定性可能使sEV成为更理想的血液生物标志物,从而提高临床检测的可靠性。
sEV中的特定蛋白(如Tmem119)可用于区分小胶质细胞来源与外周免疫细胞来源的sEV。此外,尽管CD13和嘌呤能受体P2ry12在其他细胞或组织中有不同程度的表达,但在区分中枢神经系统细胞源性sEV时,它们仍然可以作为小胶质细胞的标志物。使用组学方法如蛋白质组学、转录组学、代谢组学和脂质组学筛选生物标志物的方法也越来越多地受到关注。
目前常用分离方法包括差速超速离心、密度梯度离心和尺寸排阻色谱,但仍需克服蛋白质污染、分离效率低和特异性差等问题。新型分离技术如磁珠免疫捕获、纳米流式细胞术和种子扩增法正逐步提升sEV的分离效率与纯度。
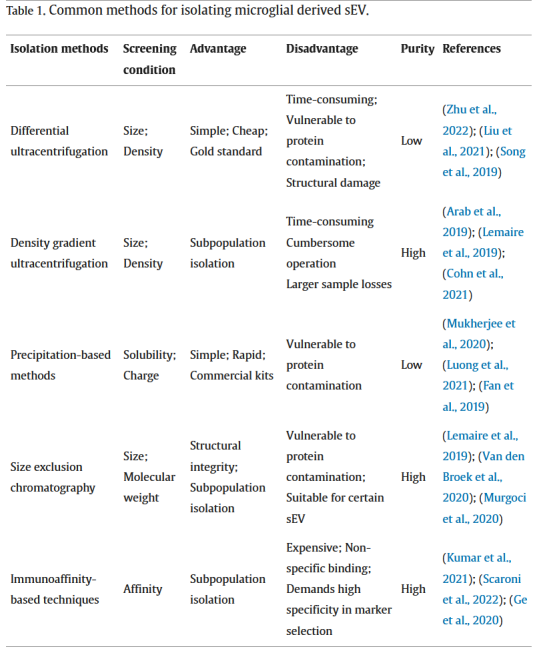
表1 分离小胶质细胞来源sEV的常见方法
然而,生物标志物的研究与应用仍面临许多挑战。生物标志物的检测方法和技术需要进一步优化,以提高检测的准确性和便捷性;现有研究主要基于小样本或动物模型,生物标志物的临床应用需要大规模的多中心临床试验来验证其诊断价值和治疗潜力;神经疾病的发生和发展机制复杂多变,单一生物标志物难以覆盖所有病情,因此需要发掘更多具有特异性和敏感性的生物标志物,以实现更为精准的诊断和治疗。
通讯作者

王玮 教授
*主任医师,博士生/博士后导师
*中国医科大学附属一院呼吸与危重症医学科主任
*中华医学会呼吸分会常委
*中国医师协会呼吸医师分会副会长
*辽宁省医学会呼吸分会主任委员
*辽宁省医师协会内科医师分会副会长
*兴辽英才计划百千万人才领军人才
*辽宁省特聘教授
*辽宁省青年名医
*辽宁省本科教学名师
*辽宁省优秀科技工作者
*辽宁省学术头雁
*辽宁省三八红旗手
*辽宁省最美医务工作者
*全国五一劳动奖章获得者
*中国好医生抗疫特别人物
第一作者

陈丽霖 博士
*在读博士
*第一作者或共同第一作者发表SCI文章3篇