恶性胸膜间皮瘤(MPM)是胸膜原发性恶性肿瘤中最常见的一种,其诊断难度较高,初诊时多为晚期。目前,针对该疾病的治疗手段较为有限,临床疗效较差,因此,MPM已成为胸膜疾病领域亟需解决的重要难题之一。广医一院/国家呼吸医学中心/广州呼吸健康研究院汪金林教授团队长期专注于胸膜疾病,尤其是恶性胸膜疾病和恶性胸腔积液的临床诊疗与基础研究,并取得了一系列重要成果。3月27日,汪金林教授团队联合暨南大学纳米研究中心陈填烽教授团队在Nano Today (IF 13.2)杂志在线发表了Translational selenium nanoparticles enhance NKG2D-mediated cytotoxicity of NK cells against malignant pleural mesothelioma cells through the TrxR1-pSTAT3 pathway的研究论文,第一作者是在读博士研究生刘少薇和硕士研究生李雪。这是国家呼吸医学中心/广州呼吸健康研究院首次发表MPM的相关研究论文,标志着胸膜纵膈疾病亚专科在MPM这一难题研究方面取得了显著的进展。
针对MPM的治疗,培美曲塞联合铂类化疗作为一线治疗方案的疗效存在局限性;近年来获批的“双免疫联合疗法(纳武利尤单抗+伊匹木单抗)”进展难言突破。究其原因,MPM复杂的肿瘤免疫微环境是关键因素。一方面,MPM呈现的”冷肿瘤”免疫状态导致以T细胞活化为核心的免疫疗法疗效有效;另一方面,MPM引起的类似石棉的“坚硬”的胸膜增厚,形成了物理屏障,使得众多药物难以有效渗透至病灶区域。针对这一特征,团队以MPM的肿瘤免疫微环境为切入点,深入分析并发现了其微环境中存在显著的微量元素硒缺乏现象。基于此,团队创新性地应用已经成功开发的具有免疫激活功能的纳米硒香菇多糖(LET-SeNPs),独辟蹊径,聚焦于NK细胞的调控机制。研究表明,LET-SeNPs能够显著提升胸腔积液中NK细胞的比例,并通过TrxR1-pSTAT3通路增强NKG2D介导的NK细胞对MPMD细胞的细胞毒性作用,从而实现高效的肿瘤杀伤效果。这一研究成果为LET-SeNPs在临床转化中的应用奠定了坚实的理论基础(图1)。可谓是“胸膜间皮瘤,坚不可摧,纳米材料来攻坚”。

图1. LET-SeNPs增强NK细胞介导的抗MPM活性机制示意图。
首先,汪金林教授团队充分利用近年来形成的“微创胸膜活检”这一专科技术优势,对MPM进行微创且精准的诊断。在此基础上,团队进一步深入研究了确诊病例中MPE的肿瘤免疫微环境,揭示了硒元素及其相关蛋白(SEPP1)的缺乏现象。研究还发现,这些缺乏与NK细胞的功能密切相关,而与T细胞功能之间的关联性相对较弱(图2)。

图2. MPM患者胸腔积液中硒元素及其相关蛋白的水平。
根据前面的研究发现,团队随后将已经成功开发的、具有免疫激活功能的LET-SeNPs应用于MPE的治疗。该纳米颗粒在MPE微环境中可降解释放出硒元素,从而缓解MPE中的硒缺乏现象。此外,LET-SeNPs表现出很好的药物渗透性能,能够有效穿透MPM类器官发挥其作用(图3)。
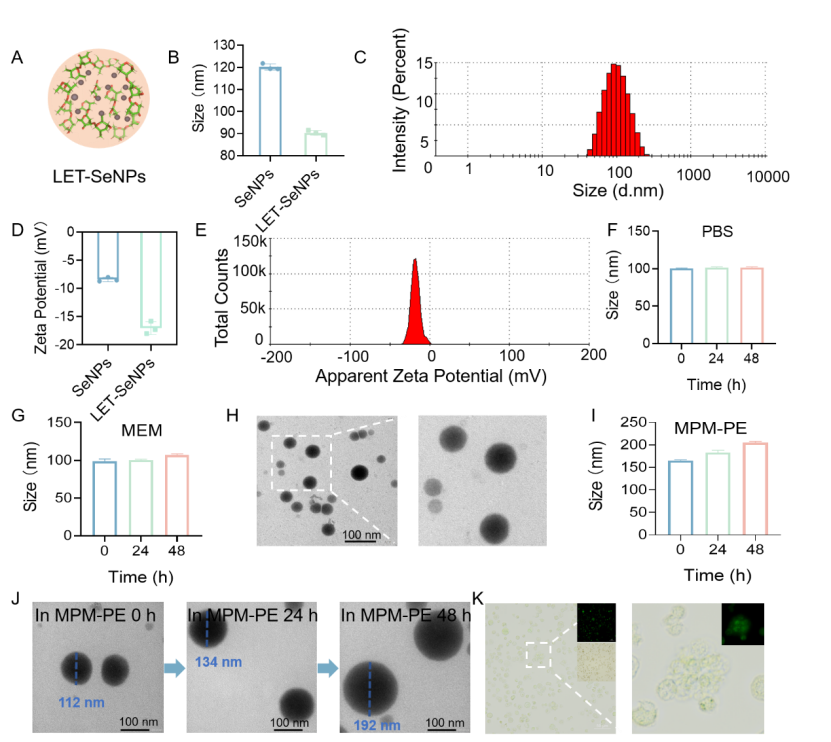
图3. LET-SeNPs能够在MPE中释放硒元素,展现出良好的渗透性,可在类器官中发挥其作用。
为进一步探索LET-SeNPs在MPM中的应用潜力,团队采用LET-SeNPs预处理的NK细胞对MPM肿瘤球进行深入研究。结果表明,经LET-SeNPs预处理的NK细胞对MPM肿瘤球表现出显著的渗透能力,并且其渗透效果与处理时间呈正相关关系。此外,侵袭实验结果显示,LET-SeNPs预处理的NK细胞能够显著抑制间皮瘤细胞的侵袭能力,同时MMP-2表达水平明显下降。上述研究表明,LET-SeNPs与固有免疫细胞NK细胞的协同作用在抗MPM治疗中展现出潜在的重要价值(图4)。

图4. LET-SeNPs预处理的NK细胞能够显著抑制间皮瘤细胞的侵袭能力,MMP-2表达水平明显下降。
为了深入探讨LET-SeNPs如何激活NK细胞功能并发挥其作用,团队最后采用了嵌入式共培养实验进行系统性研究。结果显示,LET-SeNPs增强了NK细胞的迁移能力,并在与间皮瘤细胞接触时表现出更强的细胞毒性。进一步实验表明,NK92细胞上活化性受体NKG2D表达水平上调。具体机制为,LET-SeNPs通过调控TrxR1-pSTAT3信号通路触发NKG2D受体的激活,从而通过NKG2D-NKG2DL相互作用模式实现NK细胞毒性的增强(图5)。
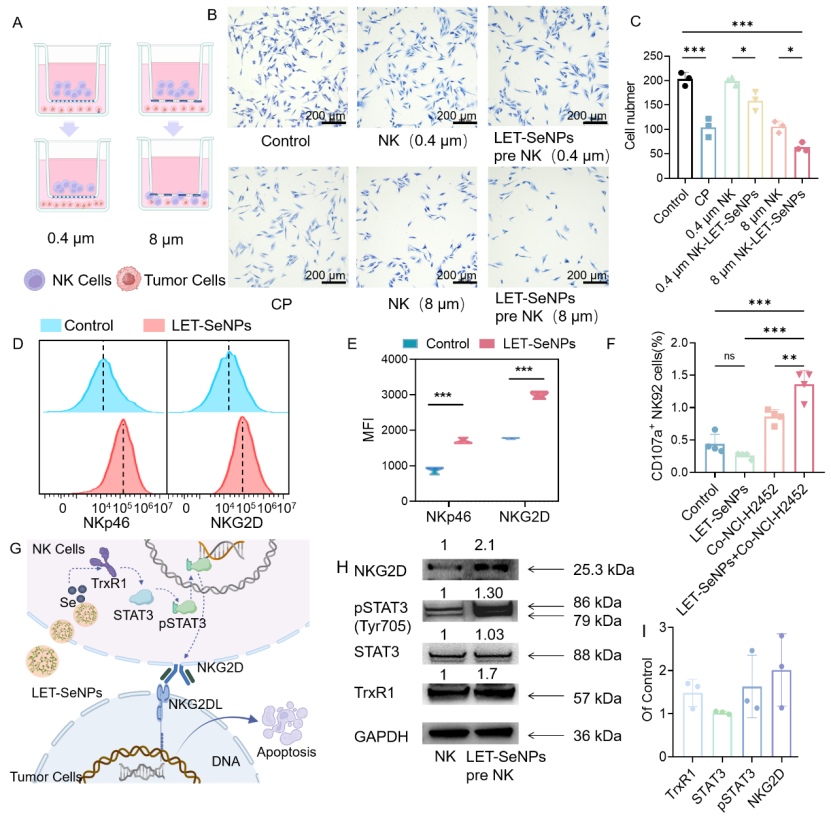
图5. LET-SeNPs通过TrxR1-pSTAT3信号通路触发NKG2D受体的激活,通过NKG2D-NKG2DL相互作用模式实现NK细胞毒性的增强。
【总 结】
基于MPE的肿瘤免疫微环境机制探索创新治疗策略是本团队近年来的重点临床基础结合研究的尝试。本团队与暨南大学陈填烽教授团队联合,应用纳米医学的技术,改善间皮瘤患者胸腔积液内复杂的微环境,纳米硒在激活NK细胞并增强免疫治疗中的应用具有巨大的潜力,为肿瘤治疗提供了新的策略和方法。
【通讯作者】

汪金林教授,主任医师,研究生导师
*广州市呼吸质控中心秘书,广东省医学会呼吸分会秘书,广东省胸部疾病学会胸膜纵隔疾病专委会主任委员,国家呼吸中心/呼吸健康研究院胸膜与纵隔疾病病区主任,广州医科大学附属第一医院呼研院第四党支部书记。
*致力于胸膜疾病,恶性胸腔积液的诊治与研究。在Adv Mater、AFM、AHM、JNB、Nano Res、Nano Today等高水平杂志(>10分)发表文章8篇,封面文章2篇。主持科技部四大慢性重点专项子项目1项、广东省自然科学基金面上课题2项、广州市科技计划和广东省推广项目各1项。
*中华医学会重症医学分会委员
*入选2012-2021年全国呼吸与危重症医学领域学者论文学术影响力排名100强。胸膜相关研究入选梅斯医学“2024年中国十大医学研究”之一。
论文信息
Translational selenium nanoparticles enhance NKG2D-mediated cytotoxicity of NK cells against malignant pleural mesothelioma cells through the TrxR1-pSTAT3 pathway.Shaowei Liu✝, Xue Li✝, Weifeng Wei, NaiJian Li, Ligeng Xu, Wei Huang, Yunxiang Zeng, Tianfeng Chen*, and Jinlin Wang*NANO TODAYDOI: 10.1016/j.nantod.2025.102720论文链接:https://doi.org/10.1016/j.nantod.2025.102720