
近日,广州医科大学附属第一医院何建行/梁文华教授团队在权威期刊柳叶刀-肿瘤学(Lancet Oncology,IF=41.6)发表了一项多模式荟萃分析,对目前所有免疫治疗相关策略在EGFR突变非小细胞肺癌(NSCLC)一线靶向治疗耐药后患者人群中的使用进行了深度解析。结果表明:免疫联合抗血管治疗与化疗的组合(ICI-antiangio-chemo)表现出最佳的无进展生存期,文中对相应疗效预测标志信息进行了探索以进行更好的有效人群筛选。
【研究亮点】
1. 本研究基于最新数据进行了最全面的评估。挑战了当前临床实践中认为ICI对具有免疫惰性特征的EGFR突变NSCLC疗效有限的观点。提出这种观点主要适用于ICI单药治疗,而对于某些基于ICI的联合治疗或可改变对这一难治人群临床决策和治疗指南。亚组分析的结果也为人群的精准用药提供了优化依据。
2. 在已有数据量不算充足的情况下,应用多模式荟萃 高级别优化方法,充分 运用了包括多臂临床研究以及大量单臂临床研究的数据,从而提高了研究的稳健性和可靠性。这也是Lancet Oncology杂志首次发表这种文章类型。
3. 这是团队承接既往在BMJ上发表针对EGFR突变晚期NSCLC一线治疗最优解探索的延续性研究,因此,经多年的不懈努力,团队对EGFR突变晚期患者一线、二线治疗完成了治疗普的描绘。多位审稿人认可研究“技术严谨且具有及时性”, “这是一项巨大的工作,需从众多研究中提取数据,汇总主要数据,将其整合,并使用相当复杂的技术进行分析”,“具有解决临床问题的巨大潜力”。
【研究背景】
EGFR突变NSCLC在接受EGFR-TKI治疗耐药后常会进入无良药可用的境地,这一庞大的人群在临床中广泛受到关注和担忧。尽管ICI治疗在NSCLC治疗中的应用飞速扩展,其在EGFR突变患者人群中的有效性仍存在争议。
【研究方法】
研究团队在2024年1月31日前已发表和未发表的I、II或III期临床试验数据(涵盖17项单臂试验和15项随机对照试验共2886名患者),多角度评估了ICI治疗相关策略在EGFR突变晚期NSCLC患者EGFR-TKI靶向治疗耐药后的疗效和安全性,主要终点指标是无进展生存期(图1)。
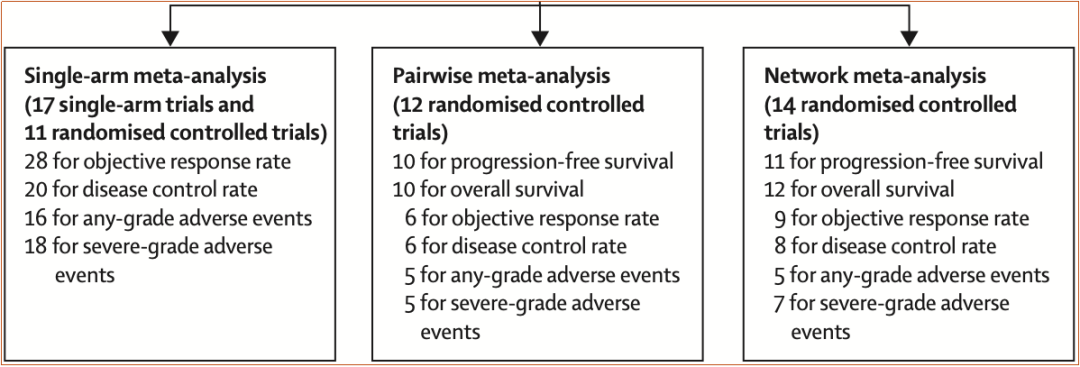
图1. 纳入研究及评估终点
【研究结果】
针对这一耐药人群,本研究基于最新数据全面评估了7种不同的免疫相关治疗策略:免疫单药、免疫联合化疗、免疫联合抗血管治疗、免疫联合抗血管治疗加化疗、双重免疫、双重免疫加化疗、免疫联合EGFR-TKI。挑战了当前临床实践中免疫对这一难治人群疗效有限的观点。提出这种观点主要适用于免疫单药治疗,而免疫联合化疗相较单纯化疗显著延长了患者无进展生存期,额外再加入抗血管治疗可进一步改善预后,但相应毒性的增加虽可接受但也需在临床实践中关注。亚组分析的结果也为人群的精准用药提供了优化依据。
Single-arm荟萃分析
在所有ICI治疗策略中,总客观缓解率为29.0%(95% CI 21.3−36.7,I2=94%),疾病控制率为77.7%(69.9−85.4,I2=93%)。其中,ICI-antiangio-chemo客观缓解率【60.6%(51.0−70.2,I2=76%)】与疾病控制率【94.6%(89.4−99.7,I2=78%)】最为理想,其次是ICI-chemo,其客观缓解率为35.8%(28.1−43.4,I2=69%),疾病控制率为82.8%(80.1−85.5,I2=16%)。
Pairwise荟萃分析
相比化疗,ICI单药治疗未延长无进展生存期(HR 1.73,95% CI 1.30−2.29,I2=0%),但ICI-antiangio-chemo(HR 0.54,95% CI 0.44−0.67,I2=0%)和ICI-chemo(HR 0.77,95% CI 0.67−0.88,I2=0%)均延长了无进展生存期(图2)。
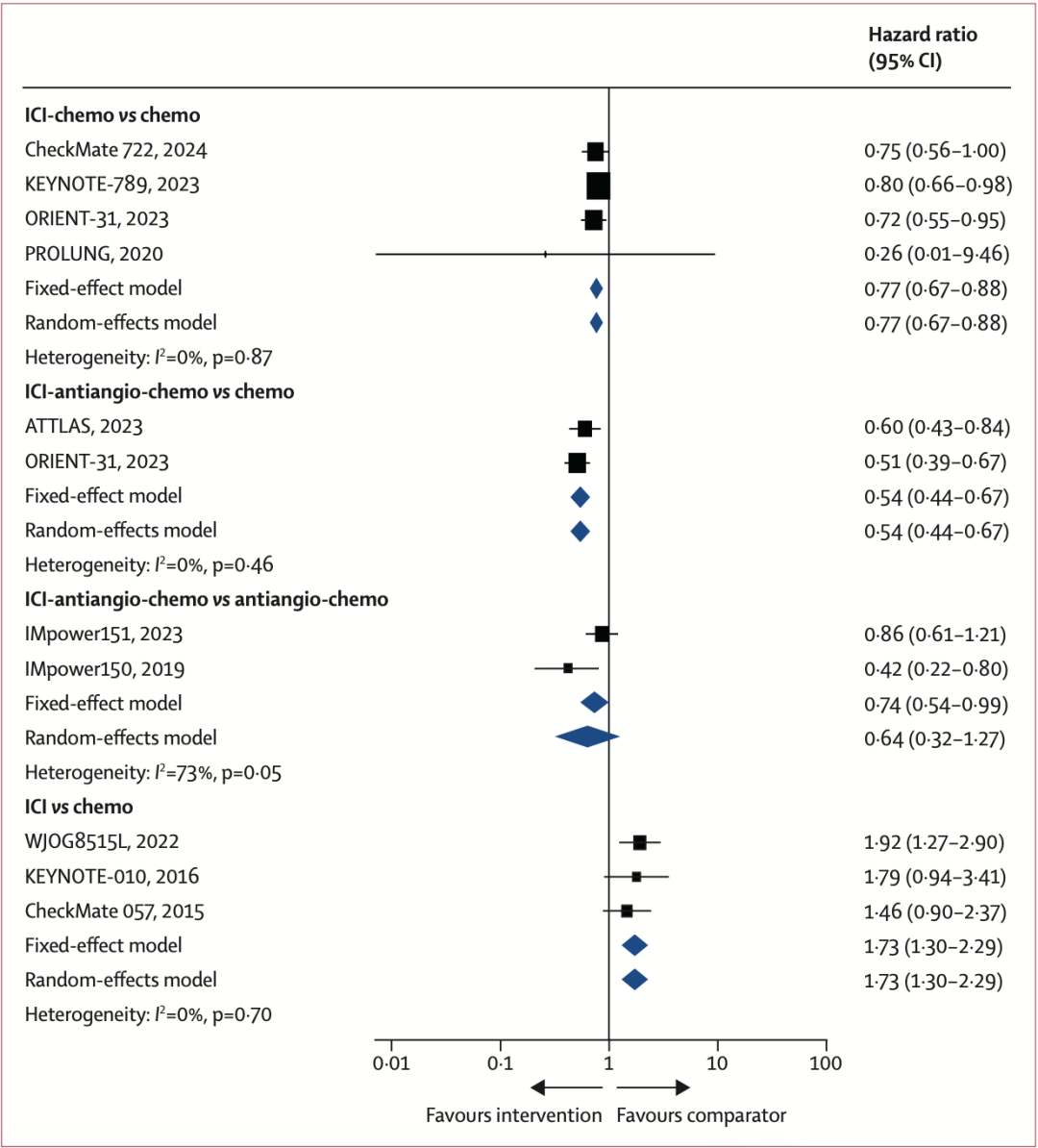
图2. Pairwise荟萃分析中各组头对头比较的合并无进展生存期
Network荟萃分析
在可比较的所有治疗中(图3),ICI-antiangio-chemo显示了最佳的无进展生存期结果,明显优于:ICI-chemo(HR 0.71,95% CrI 0.59−0.85)、ICI单药(HR 0.30,95% CrI 0.22−0.41)、 Antiangio-chemo(HR 0.76,95% CrI 0.58−1.00)、单纯化疗(HR 0.54,95% CrI 0.45−0.64)。然而,ICI-antiangio-chemo相较于ICI-chemo和单纯化疗,具有更高的任何级别和3级或更严重的不良事件风险。
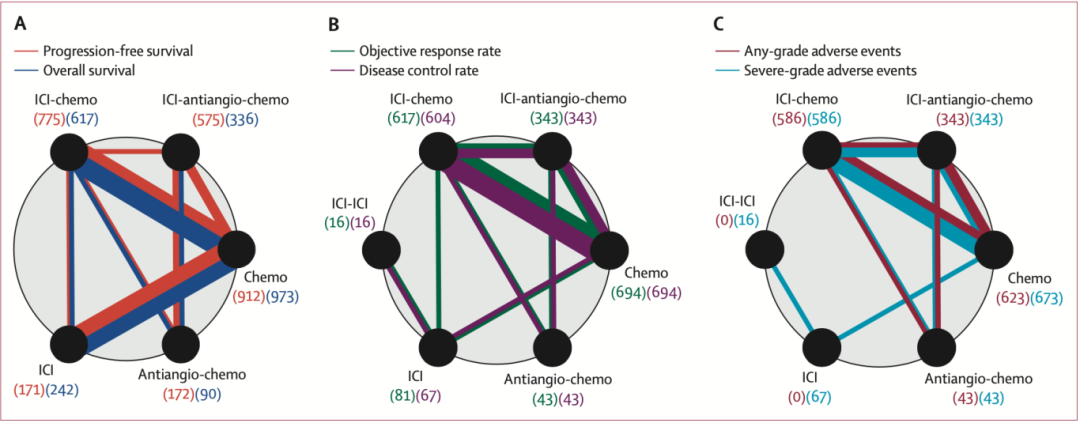
图3. Network荟萃分析中各治疗组间的比较模式

图4. Network荟萃分析中各治疗组间疗效和安全性的比较结果
总之,针对EGFR突变NSCLC一线靶向治疗耐药人群,ICI联合化疗相较单纯化疗显著改善了患者预后,额外再加入抗血管治疗可进一步延长无进展生存期,但相应毒性的增加虽可接受但也需在临床实践中关注。
【研究团队】
通讯作者:何建行教授、梁文华教授(广州医科大学附属第一医院)
共同第一作者:赵毅、何映、王炜、蔡棋(广州医科大学附属第一医院)、葛帆(中国医学科学院肿瘤医院)、陈子盛(清远市人民医院)
参考文献:
[1] Zhao Y, He Y, Wang W, Cai Q, Ge F, Chen Z, Zheng J, Zhang Y, Deng H, Chen Y, Lao S, Liang H, Liang W, He J. Efficacy and safety of immune checkpoint inhibitors for individuals with advanced EGFR-mutated non-small-cell lung cancer who progressed on EGFR tyrosine-kinase inhibitors: a systematic review, meta-analysis, and network meta-analysis. Lancet Oncol. 2024 Aug 16:S1470-2045(24)00379-6. doi: 10.1016/S1470-2045(24)00379-6. Epub ahead of print. PMID: 39159630.
[2] Zhao Y, Liu J, Cai X, Pan Z, Liu J, Yin W, Chen H, Xie Z, Liang H, Wang W, Guo Z, Zhao S, Liang W, He J. Efficacy and safety of first line treatments for patients with advanced epidermal growth factor receptor mutated, non-small cell lung cancer: systematic review and network meta-analysis. BMJ. 2019 Oct 7;367:l5460. doi: 10.1136/bmj.l5460. PMID: 31591158; PMCID: PMC6778694.